Nuove scoperte sull’origine dell’emicrania
L'emicrania, la terza malattia più comune a livello globale, causa un dolore intenso e invalidante, spesso accompagnato da nausea, vomito e estrema sensibilità alla luce e al suono. Circa una persona su sette soffre di emicrania, che può durare da ore a giorni. Le scoperte di un recente studio aprono le porte a nuove strategie terapeutiche.
Una mutazione specifica associata all'emicrania aumenta l'eccitabilità neuronale
L'emicrania, la terza malattia più comune a livello globale, causa un dolore intenso e invalidante, spesso accompagnato da nausea, vomito e estrema sensibilità alla luce e al suono. Circa una persona su sette soffre di emicrania, che può durare da ore a giorni. Le scoperte di un recente studio aprono le porte a nuove strategie terapeutiche.
Mutazioni genetiche e fattori ambientali giocano un ruolo critico nell'insorgenza dell'emicrania. Uno studio pubblicato all'inizio del 2018 sulla rivista Neuron ha mostrato perché alcune famiglie siano sensibili all'emicrania e come la genetica possa influenzare il tipo di emicrania di cui soffrono. Sono state identificate 44 varianti genetiche che potrebbero essere correlate all’emicrania, ma al momento nessuna di queste varianti è stata correlata specificamente ai diversi tipi di emicrania.
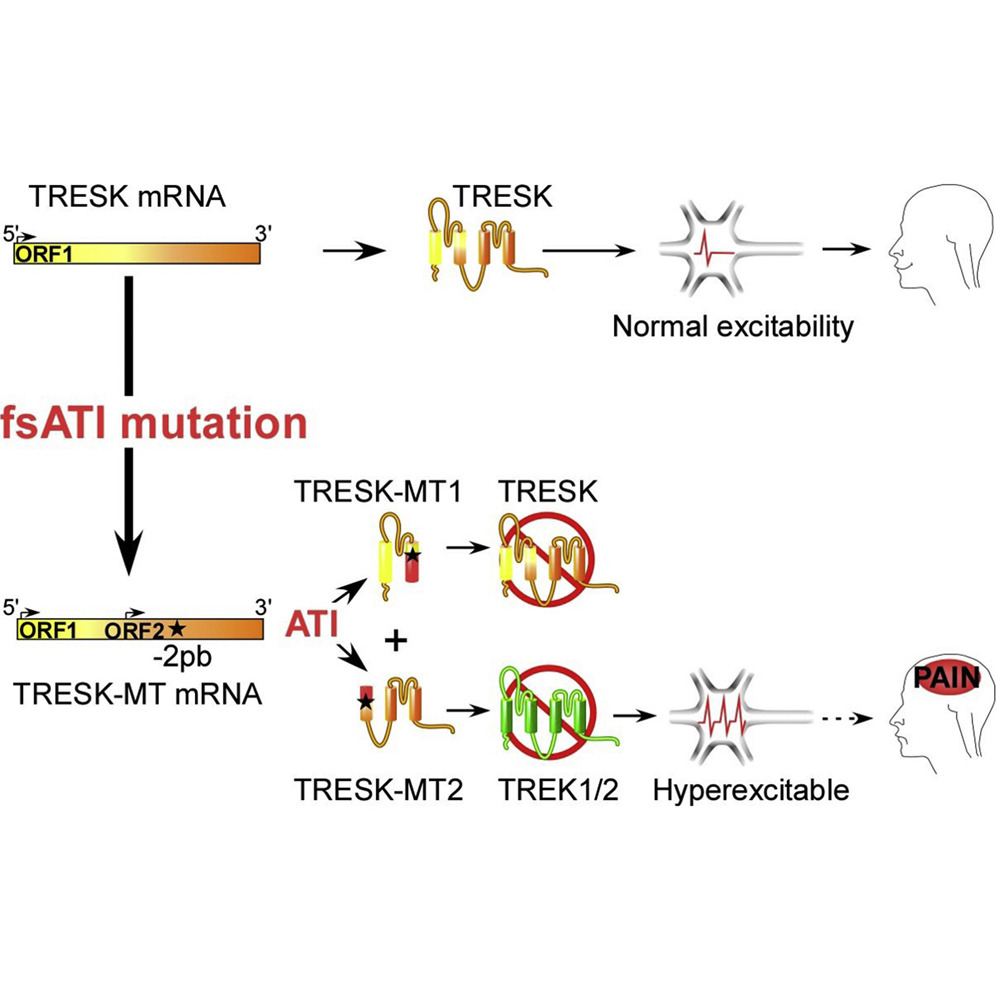
Recenti scoperte hanno identificato un ruolo potenzialmente importante dei canali di potassio a due pori (K2P) nello sviluppo del dolore tipico dell’emicrania. In particolare si è scoperto che TRESK, un sottotipo di canale K2P espresso dai neuroni sensoriali, potrebbe essere coinvolto nella genesi dell’emicrania con aura. La mutazione TRESK-MT induce ipereccitabilità dei neuroni trigeminali, mentre un'altra mutazione di TRESK, TRSEK-C110R, ha effetti negativi sull'emicrania.
Gli effetti opposti sull'emicrania dalle mutazioni TRESK hanno spinto un team di ricerca francese ad indagare il ruolo esatto di TRESK nella genesi dell’emicrania. Lo studio condotto sui topi ha identificato che la mutazione TRESK-MT inibisce i canali TREK1 e TREK2, anche loro canali K2P coinvolti nell’eccitabilità dei neuroni trigeminali e quindi potenzialmente in grado di scatenare emicrania. La mutazione TRESK-C110R, invece, si è scoperto non regolare i canali TREK. Questi risultati, pubblicati su Neuron lo scorso 17 dicembre, aprono nuove strade per produrre farmaci contro l’emicrania. L'obiettivo è quello di indirizzare il farmaco verso i canali TREK 1/2 per ridurre l'attività elettrica dei neuroni e prevenire l'insorgenza dell'emicrania.
I ricercatori propongono che questo nuovo meccanismo genetico, per il quale la stessa mutazione causa la formazione di due proteine invece di una sola, debba essere considerato nello studio di altre malattie genetiche e per la loro diagnosi.
Fonte: Royal P, Andres-Bilbe A, Ávalos Prado P, Verkest C, Wdziekonski B, Schaub S, Baron A, Lesage F, Gasull X, Levitz J, Sandoz G. Migraine-Associated TRESK Mutations Increase Neuronal Excitability through Alternative Translation Initiation and Inhibition of TREK. Neuron. 2018 Dec 12. pii: S0896-6273(18)31048-1. doi: 10.1016/j.neuron.2018.11.039.